相异构想:
1、由于学生对之前所学的盐类水解和溶液这部分知识的遗忘,可能会忘记如何分析水中粒子组成,忽视了像水分子这样的粒子。
2、由于电离能力在一定程度上与溶液的导电性有联系,学生会误以为弱电解质的导电能力比强电解质差,或者简单地用电离常数比较导电能力,这些都是错误的想法。
3、学生可能会把弱电解质的初始浓度误以为是平衡浓度,影响电离平衡常数的计算。学生可能会溶液中的离子浓度不会受到溶质初始浓度的影响
4、学生可能加深弱电解质分步电离的概念,而忽略各级电离平衡常数相差数量级较大,在计算方面可以选择性忽略。
5、在学习影响弱电解质电离的因素时,由于部分学生三重表征掌握不到位,难以将宏观现象与微观粒子运动相结合,可能无法理解强电解质是如何对弱电解质产生影响
6、在进行分析时,如果增大弱电解质溶液的浓度,学生可能认为其化学反应速率的大小和解离度解离度都应该增大。
7、弱电解质电离平衡中,学生可能会忽略温度对溶液中离子浓度的影响。
8、弱电解质电离平衡中,离子的迁移速率与离子的电荷无关。
9、弱电解质电离平衡中,电离度与溶液的酸碱性无关。
http://www.dxsbao.com/xiaonei/657314.html
点此复制本页地址
为深化生态文明教育,引导师生树立环保理念,以实际行动践行绿色发展理念,助力校园文明建设,4月16日下午,沈阳城市学院第八届“绿岛春‘锋’行,美景共绘就”主题环境文化节总结表彰大……
沈阳城市学院 沈阳城市学院校学生会查看全文 >>
本网讯(校团委李家毅)2025年4月21日17时30分,公路喜剧电影《苍茫的天涯是我的爱》主创团队受邀现身沈阳城市学院绿岛讲堂,举办校园路演活动。导演陈孝良携演员曾毅、周奇、赵海燕、张智超……
沈阳城市学院 沈阳城市学院校学生会查看全文 >>
本网讯(校团委张嘉琪)为丰富校园生活,增强学生体质,培养团队协作精神,深化校企合作,2025年3月21日15时,由康师傅独家赞助的篮球总决赛于沈阳城市学院玫瑰园篮球场圆满举办。此次活动……
沈阳城市学院 沈阳城市学院校学生会查看全文 >>
本网讯(校团委李家毅张嘉琪)为进一步学习党的二十大精神、贯彻落实习近平新时代中国特色社会主义思想,鼓励沈阳城市学院学子积极参与到各项社会实践活动中去,践行沈阳城市学院“我行……
沈阳城市学院 沈阳城市学院校学生会查看全文 >>
本网讯(校团委李家毅)2025年4月9日13时,沈阳城市学院第十三届“雄辩绿岛”青年辩论赛半决赛于我校建工楼410教室成功举办。参赛双方分别为正方商学院与反方文化与传播学院,五大学院的学生……
沈阳城市学院 沈阳城市学院校学生会查看全文 >>
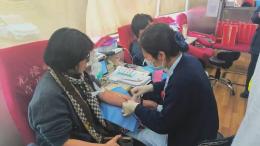 本网讯(校团委牛康莉)2025年3月26日13时,由沈阳中心血站联合我校举办的无偿献血活动于南楼成功开展。活动开展期间,广大师生纷纷踊跃参加,用热血传递爱心,以行动诠释担当。为确保此次……
沈阳城市学院 沈阳城市学院文化与传播学院查看全文 >>
本网讯(校团委牛康莉)2025年3月26日13时,由沈阳中心血站联合我校举办的无偿献血活动于南楼成功开展。活动开展期间,广大师生纷纷踊跃参加,用热血传递爱心,以行动诠释担当。为确保此次……
沈阳城市学院 沈阳城市学院文化与传播学院查看全文 >>
校团委(本网讯李家毅)为进一步提升我校校学生会学生干部的综合素质,加强团队协作与凝聚力,2024年11月13日13时,校团委于我校三期操场开展学生干部素质拓展活动,此次活动由文体部策划筹……
沈阳城市学院 沈阳城市学院查看全文 >>
本网讯(校团委潘姝宁李家毅张冰)为进一步学习党的二十大精神、贯彻落实习近平新时代中国特色社会主义思想,2024年10月22日,沈阳城市学院2024年“青春为中国式现代化挺膺担当“暑期社会实……
沈阳城市学院 沈阳城市学院查看全文 >>






